荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
生物医学研究和应用中动物实验的减少(Reduction)、优化(Refinement)和替代(Replacement)的3R原则提出60多年来已逐渐得到普及并成为共识,技术人员也愿意关注实验动物的福利伦理并主动实践减少和优化的2R原则。但以替代为核心的1R原则由于投入和研发时间长难度大一直以来进展缓慢。进入21世纪后,现代生物技术的飞速发展推动毒理学测试走向现代化,替代动物实验的1R原则进入快速轨道。欧盟关于化妆品动物实验禁令的实施和化学品REACH法规的影响,以及之后越来越多的国家将替代动物实验列为化妆品法规,推动了替代技术的监管认可。近年来,以美国为首推行的“21世纪毒性测试观念与远景”,使得大量体外新技术从基础研究转化为体外方法应用于皮肤生物学和化妆品领域。

程树军博士研究员 广东检验检疫技术中心
1. 非动物检测方法分类
凡是利用无知觉材料(如计算机模型、体外细胞、重建组织、离体器官、低等生物等)替代活体哺乳动物的安全性与功效性的测试都可称为体外方法。根据实验系统和使用目的,体外方法可分为三类。
1.1. 非测试方法
非测试方法(Non-testing methods)又称为“硅片方法”(In silico methods),广义是指任何基于计算机开发的预测方法。基于计算机的强大功能,很多毒性测试与功效评估的计算机方法被开发出来,用于预测化合物对人体健康和环境的影响,例如定量构效关系(QSAR)分类法,交叉参照(Read-across)、毒理学阈值(TTC)和专家系统等。这些方法在经济合作与发展组织(OECD),欧盟、美国和日本等国家和地区发展较快,例如已经有不少QSAR 模型和工具应用到化妆品毒理学安全性评估中,例如,OECD QSAR Toolbox、Toxtree、CAESAR、TEST 及HESS 等,毒性终点涉及经皮吸收、皮肤刺激、眼刺激、皮肤致敏、急性毒性、重复剂量染毒、生殖发育、遗传和致癌等。欧盟消费者委员会(SCCS)认为针对化妆品杂质及含量极小的化妆品原料安全性评估,可以使用TTC 方法。在工业化学品领域,交叉参照作为非测试方法中的重要一员已被多个国家的管理机构所接受。我国国家食品药品监督管理总局(CFDA)发布的《化妆品新原料申报与审评指南》中也提到:可以根据该原料理化特性、定量构效关系、毒理学资料、临床研究、人群流行病学调查以及类似化合物的毒性等资料情况,增加或减免试验项目。交叉参照方法也被中国新化学物质申报登记指南所认可。总的来说,中国化妆品非测试方法的限解刚起步,开发和应用与国外都还存在一定的差距,还需要更多的经验积累和借鉴。
1.2. 替代方法
狭义的替代方法是指经过科学验证程序证明其相关性和可靠性,用于替代传统动物实验并被监管机构所认可的体外方法。因此,替代方法的结果应当与预期回答的毒性终点之间建立预测关系,即体外实验获得的数据与体内动物效应之间建立统计学模型。如体外细胞毒性预测啮齿类动物的急性经口毒性,在细胞活性的半数抑制浓度(IC50)与动物半数致死剂量(LD50)间建立线性关系;基于3D表皮模型的皮肤刺激方法把细胞活性与体内刺激评分建立判定关系;眼刺激的鸡胚方法把血管反应与体内眼刺激建立相关关系等。替代方法验证工作最早始于1994年成立的欧洲替代方法验证中心(ECVAM),完成验证的方法已超过50项。
1.3. 体外方法
广义的体外方法既包括符合法规要求的替代方法,还包括大量应用于化妆品原料和产品安全性或功效性测试的体外方法。体外方法由体外实验系统、实验过程、指标及检测方法、结果和统计方法(预测模型)等4个基本要素组成,还包括实验原理、适用范围等界定方法应用领域的因素。如美白剂的整合测试策略组合了酪氨酸酶抑制、B16 或人黑色素细胞生成抑制、角质细胞摄取试验、斑马鱼测试等多个体外方法(表1),抗光老化功效的体外测试组合包括酯酶抑制方法,成纤维细胞光老化测试和三维重建皮肤模型的方法等。这类方法紧跟皮肤生物学的发展,且与检测技术和装备的进步密切相关,因而新技术不断涌现、个性化方案很多,为产品的宣称提供数据支持。
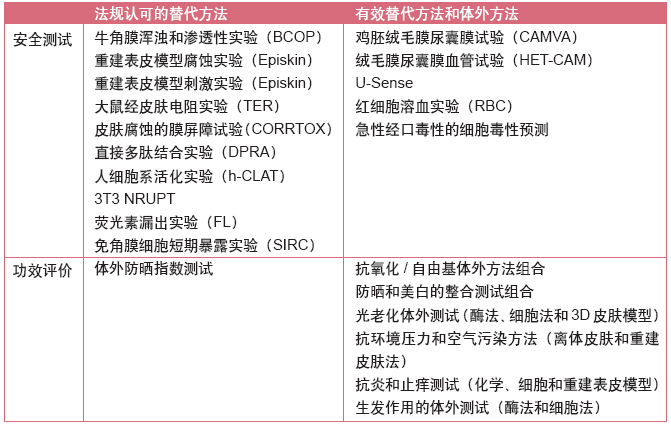
表1. 目前国内使用的体外方法
2. 化妆品体外测试新技术进展
首个法规认可的替代方法是OECD2004年发布的指南432,即3T3中性红摄取光毒性试验(3T3NRUPT),目前列入指南的方法已经超过20项。我国接受替代方法成为国家标准和检验检疫行业标准(SN)始于2006年,累计发布标准约30项,CFDA在2016年10月吸收列入《化妆品安全技术规范》的首个替代方法是3T3 NRUPT。截止目前,OECD先后发布的替代方法已覆盖皮肤吸收、光毒性、眼刺激、皮肤刺激、皮肤致敏、遗传毒性、内分泌干扰等毒性终点。如目前已在国内应用的BCOP、EPIOSKIN、DPRA 等。常用于化妆品评测的体外方法如表1。
近年来,体外方法的发展呈现三个趋势。一是研发重点转向更复杂的毒理学领域,如皮肤致敏、肝脏毒性、生殖发育毒性和内分泌干扰等,如2016年发布的DPRA、h-CLAT。二是整合策略的开发,尝试把单一的方法合理科学地组合使用。如已发布的眼刺激IATA,皮肤刺激IATA草案和研究中的皮肤致敏IATA。整合策略不仅考虑了现有有效的方法,还加入了QSAR、理化信息、人群暴露等。而且基于大数据的分析,可以建立从体外数据直接预测人体风险的模型。三是建立基于证据的功效测试体外方法,把大量基础研究投入产出的方法转化为行业可以使用的标准,并在此基础上建立整合策略,提高功效测试数据的可重复性和科学性,满足化妆品行业发展的需要。
3. 化妆品体外测试方法应用案例分析
体外技术首先被应用于毒性分类和产品安全性分析,使传统以形态学观察为主的半定量动物实验走向以量化的生物学参数为主的体外测试,不仅提高了测试通量,而且测试结果更为客观和具有可比性。以BCOP为例说明替代方法在化妆品及相关行业的应用。
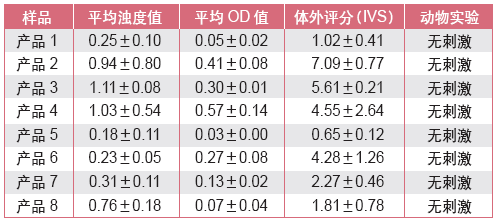
表2. BCOP 用于市售产品的检测
3.1. 标准BCOP方法
BCOP采用牛角膜作为实验系统,将其固定于特定支架。检测液体物质时,直接将样品作用于角膜10min,然后去除受试物,恒温条件下后孵育2h,测量浊度值和荧光素漏出量(OD值)。检测固体物质时,直接将样品作用于角膜4h,去除受试物后,测量浊度值和OD 值。预测模型为:体外评分(IVS)= 浊度值+15×OD值。判定依据为:IVS ≤ 3为不分类(无刺激);IVS > 3,且≤ 55为刺激性(分类2A和2B);IVS > 55为严重刺激性(分类1)。BCOP被列为OECD指南437,用于化学品腐蚀性/ 严重眼刺激性和无分类的鉴定和标识。BCOP方法的优点:完整保留角膜结构;检测指标包括屏障功能受损和基质蛋白变性,参数全面;三维结构可直接加样,不受测试样品溶解性、颜色等物理性质限制;基于角膜的测试结果在眼刺激的整体评估中权重最高,在整合策略中处于核心地位;实验方案可根据实际需要优化调整。
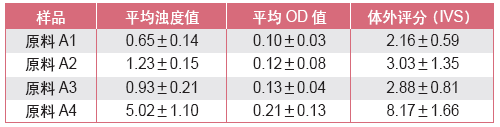
表3. BCOP 用于原料的检测
3.2. 用于市售化妆品监管
表2列举了8种市售化妆品的抽查结果,主要为眼影、眼霜、睫毛膏、沐浴液、染发剂等眼部接触产品。根据OECD方法的判定依据,除了产品1、5、7外,其他5种产品均为轻刺激性,但动物测试均为无刺激性。说明BCOP 方法比动物实验敏感,再分析每个产品的测试数值,发现浊度值和OD值尚有改善的空间,可以在产品开发阶段调整配方,使产品达到BCOP的标准。
3.3. 用于原料、配方的优化和比较
利用BCOP的测试结果可将其用于化妆品原料筛查。对于化妆品原料A,不同供应商的测试结果存在较大差异。从表3可见,A1和A3无刺激性,可优先选择。BCOP也可用于产品开发阶段不同配方的测试,通过比较不同配方的浊度值、OD值和体外评分,确定最温和的产品。对于数据比较高的配方,可通过降低某种物质的含量、去除某个成分或改变配合比例对配方进行优化。
3.4. 用于特殊人群和温和产品的测试
通常认为体外评分越小的产品越温和,因此BCOP可用于特殊人群产品的宣称,如婴童、女性、老人等,这些产品以低刺激性或温和为追求目标,如某品牌儿童产品在配方研制阶段的检测结果见表4。不断调整配方过程中,先把体外评分降到3以下,再进一步精细化工艺或配方,把OD值降到0.05左右,把浊度值降到0.1左右,使体外评分降到1以下,满足产品温和宣称的要求。经过调整后的配方5和6是比较温和的产品。
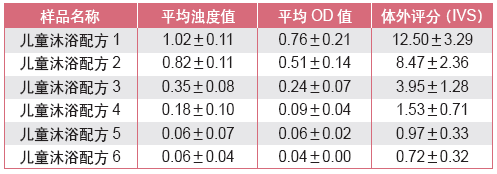
表4. BCOP 用于温和宣称产品的检测
3.5. 特殊方案的BCOP方法
为了适应产品差异化竞争、温和宣称及特殊人群的需要,需要对标准化替代方法进行优化。BCOP 的改良方法有以下几种:①多参数的BCOP:在浊度和OD 值之外增加组织学定量评分,把评分在3 ~ 55 的数值进行区分,目的是为了更精确的区分刺激性和了解受试物对组织结构的影响。②延长暴露时间的BCOP:把受试物的暴露时间从标准的10 min延长至20min或更长,再进行2 h 后孵育,目的是评价长时间接触眼角膜或上皮的刺激作用。该方案常用于长期使用的护肤品/ 眼霜、驻留类产品、医用生物材料的评估。③多重暴露的BCOP:在角膜室温平衡30 min后开始加样,连续3 ~ 4次暴露,每次10 min,间隔孵育30 min,最后测量浊度值和OD值。目的是了解受试样品多次接触角膜的刺激作用,多用于反复使用的护肤品/ 眼霜、眼部药品、护理套装的检测。④延长暴露后孵育时间的BCOP:采用常规暴露(10 min),但把后孵育延长至4 h、12 h 或18 h,测量浊度值和OD值。目的是了解受试样品单次暴露眼角膜或上皮后刺激修复作用,可用于研究含表面活性剂的物质、化妆品原料和产品、眼部药品等的刺激性。表5是对某品牌眼药科用药的刺激性评估,选择了通过三重暴露和延长时间暴露的方案,最后获得了最优化的产品。
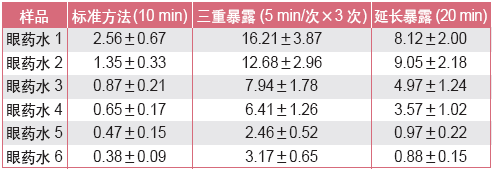
表5. 特殊BCOP 方法用于眼科用药品刺激性检测的体外评分
3.6. 用于粘膜刺激的预测
牛角膜具有上皮组织共有的结构,可将其用于粘膜(口腔、阴道)刺激和皮肤刺激性的测试。表6列举了BCOP方法检测不同漱口水产品的体外评分结果,可以发现大部分市售产品的粘膜刺激性能满足BCOP 判定要求。同样,在用BCOP 方法检测纸尿裤不同浸提液皮肤刺激性的实验中,选择了常规纯水浸提(A)、人工汗液浸提(B)和人工尿液浸提(C)3 种方式区分刺激性,为产品评价的开发提供了量化检测数据。
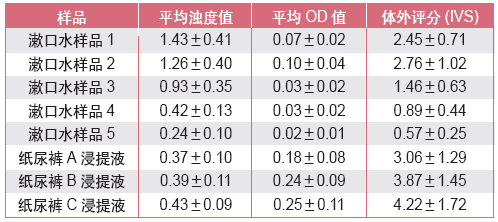
表6. BCOP 用于口腔和皮肤刺激的检测
总之,在标准化BCOP基础上的特殊方案,可满足诸如重复暴露、长时间暴露、刺激与炎症相关性等不同目的研究的需要。单一的方法还可以与CAMVA、SIRC等方法组合,弥补单一替代方法的局限性和提高预测的准确性。
4. 化妆品体外检测发展趋势
4.1. 毒性测试技术国际化
我国化妆品全安性的测试会逐渐国际化,使用与国际相同或类似的方法,或使用与国际同等水平的技术。整合运用基于风险评估资料和体外测试数据,回答原料和产品安全性和功效性的问题,把体外技术应用于整个产品制造过程。
4.2. 功效性测试多元化
功效性宣称应以安全性为前提,并应符合法规的要求。功效性的测试方法会随着科学(如皮肤生物学、肌肤结构组学、检测技术等)的发展而不断丰富和完善,如二维细胞模型、3D皮肤构建、非动物测试系统、皮肤微生物组学、临床非介入性测试设备、计算机模型、仿生技术等技术不断成熟并大量应用于化妆品评估过程中,带来了多元化的变革。
4.3. 多种评测技术融合
安全性与功效性的测试须体外与临床相结合。体外测试主要用于评估原料的有效性和安全品质,特别是对于中国传统的植物提取物,以及大量使用的化工原料,可在短时间内获得与测试相关的生物学信息,为新原料和新产品开发提供预测。临床测试(如志愿者)用于评估终产品的安全性与功效性,为产品的适应性和宣称提供直接证据。二者有机结合构成产品从研发、配方、生产到上市全过程的完整证据链。
4.4. 标准化测试与个性测试相得益彰
法规认可的替代方法多为毒性测试的标准化方法,是产品准入并应当遵循的指南。企业内部使用的替代方法可以在标准方法的水平上提高要求,或满足消费者述求,或追求更高的安全水平。例如本文举例说明的BCOP方法。随着检测数据的积累和研究的深入,许多改进方案将被行业内提出并使用。标准化与个性化检测将和谐共存服务于整个行业。