荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
方法
首先,按照1:3, 1:2和1:1的药物:聚合物比率(25%,33.3%或50%w/w浓度),干混两种组分,制备三个等级的HPMCAS(AFFINISOL™ 716G, 912G和126G,Dow Chemical Company,USA)和ITR配方。然后利用实验室双螺杆热熔挤出机(Pharma 11,Thermo Scientific,USA),在170℃,100rpm螺杆转速以及3-7g/min生产率下,通过2.0mm环形口模,加工所生成的九个配方。按照制造商推荐的HME一般应用,挤出机螺杆元件应配置两个捏合段和三个输送段。挤出物经过空气冷却并制成长度大约2mm的颗粒,然后利用配置500µm目筛和12齿转子的离心粉碎机(ZM200,Retsch,Germany),在18,000rpm转速下,研磨成粉。利用激光衍射仪(Mastersizer 2000,Malvern Instruments Ltd,UK)测定磨碎的挤出物的粒度分布。在40℃/75%RH下,粉状制剂在加速稳定条件下储存四周(开口容器)。利用差示扫描量热仪(DSC;Q200,TA Instruments,USA),在10℃/min的加热速率下进行粉末热分析,每40秒调节±2℃。利用X-射线粉末衍射仪(XRPD;Equinox 100,Thermo Scientific,USA)研究药物结晶度。利用扫描电子显微镜(SEM;Phenom XL,Phenom World,USA)观察稳定条件下储存后的药物是否存在表面再结晶。在1000mL的磷酸盐缓冲剂中,利用USP装置II,在75rpm转速下,将含有100mg药物的粉末样本进行释放度检测。
结果
粒化挤出物很容易被研磨成粉。配方的载药量能够通过改变挤出物的脆性和可研磨性能而极大地影响粒度分布。药物:聚合物比率为1:1, 1:2 和 1:3时分别获得75,120和160微米的D50值。
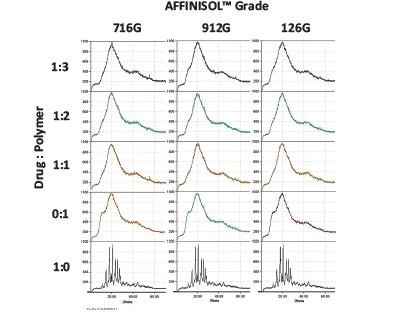
利用XRPD和DSC评估粉碎后的挤出物证实,HME配方中的ITR为无定形,而非结晶相。同时,所有配方的X-射线衍射图只观察到典型的“非晶晕环”,并未观察到ITR原料的结晶峰(图1)。这就表明,药物晶体通过AFFINISOL™ HME转化为无定形固体分散体。
图 1. ITR ASD 与组分材料的X-射线衍射图比较
此外,DSC结果表明,与未处理的药物相比,所有配方都没有结晶熔融峰(图2a和b)。DSC扫描和ASD样本显示出单一的玻璃化转变温度,表明无定形API均匀分散在聚合物中。随着ITR浓度的渐增,ASD的玻璃化转变温度(Tg)递减,究其原因是药物对所有三个等级HPMCAS的增塑作用。同时,通过增加无定形ITR浓度以及降低聚合物含量,药物聚合物比率发生变化,同样能够导致Tg降低。
图2a. 原料的DSC热分析图:结晶ITR和HPMCAS
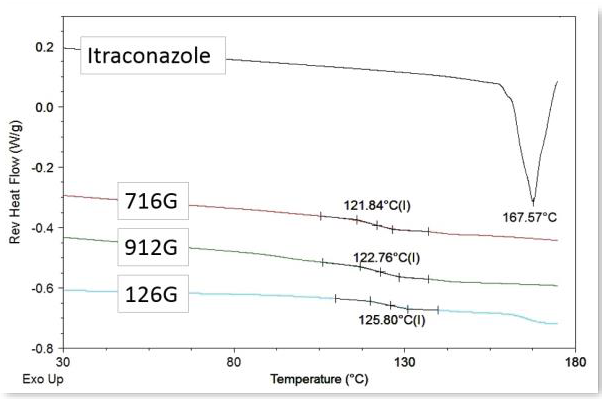
图2b. ITR ASD的DSC热分析图
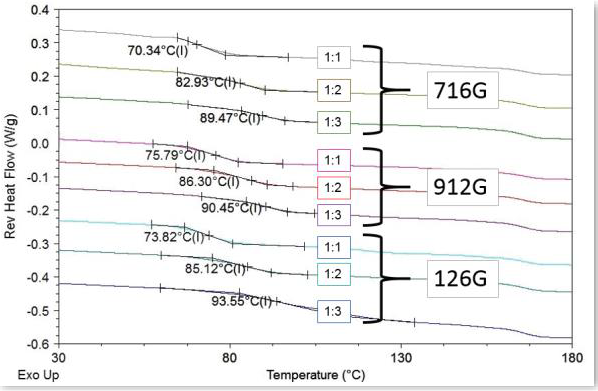
相比于结晶API或未加工的物理混合物,ASD释放度检测显示,HPMCAS 716G级和912G级组成的ITR配方的释放速率和程度明显改善。例如,包含HPMCAS 716G的ITR 配方在45分钟后释放高达90%的剂量,而类似的物理混合物仅仅释放0.3%的剂量(图3)。随着载药量的渐增,所有配方的释放速率和程度(溶解度)递减(表1)。在所有药物聚合物比率下,基于HPMCAS 716G的ASD释放速率较快,而基于HPMCAS 126G的则较慢,这可能是由于每种聚合物等级在该释放介质(pH 6.8)中的溶解度各不相同所致。而在所有配方比率下,HPMCAS 126G由于其在pH 7.0以下的介质中的溶解度很低,因此,释放几乎忽略不计。
在40℃/75% RH下,储存于开口容器中的ASD配方对药物含量测定结果影响弱甚至忽略不计,总游离酸含量(表1)以及溶解度的影响主要取决于HPMCAS等级和配方比率。其中,总游离酸含量测定结果与先前对纯聚合物的观测结果相一致,这就表明HME对聚合物的影响极小1。药物聚合物比率为1:3的716G和912G的释放曲线(储存之后)在初始时间点较慢,但与未老化样本相比,仍然能够实现一定的释放程度(溶解度)。而在较高载药量(1:2,1:1)下,HPMCAS 716G和912G配方的释放曲线(储存之后)与初始结果大致相似(f2>50)。在稳定条件下储存后,SEM图像放大900倍的颗粒表面并未观察到药物在较低载药量(1:3,1:2)时表面再结晶的迹象,虽然在1:1的颗粒表面观察到一些小的伪影,但是在随后使用XRPD或DSC进行再评估,未观察到广泛的再结晶迹象(别再现图案或熔融峰)。
表1. ITR ASD加速稳定性数据
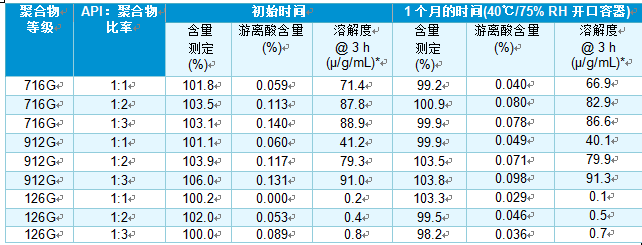
图3. 716G ASD配方(100mg剂量) vs. ITR结晶物理混合物的释放曲线
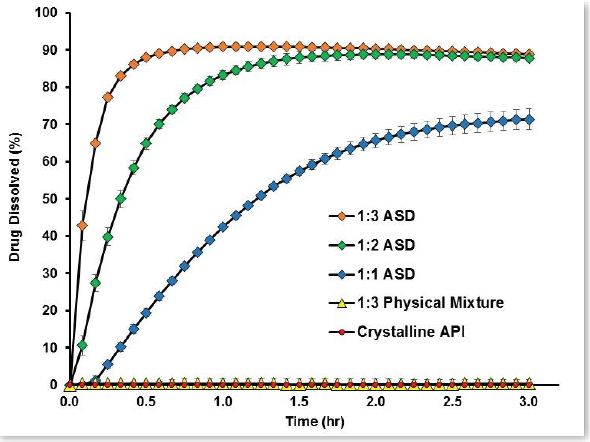
图4. 颗粒表观

结论
HME工艺能够完美地制备包含AFFINSOL™ HPMCAS的伊曲康唑无定形固体分散体,并且具有一定的载药量,而且相比未加工的物理混合物,溶解度明显增加。通过根据载药量和HPMCAS等级改变配方组成,能够实现涉及释放曲线和溶解度增加等各种不同的产品性能,同时,在加速稳定性条件下1个月的时间里仍能够保持药物为无定形形态。
参考文献
1. Martin L., Mehta R., Rane M., Cunningham C. And Rajabi-Siahboomi A. Determination of processing window for hot melt extrusion and milling of hypromellose acetate succinate by assessing thermal degradation. AAPS 2017