荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
人类微生物组(microbiome)是我们了解健康和疾病的关键所在。
这个由居住在我们肠道和全身的数万亿微生物组成的网络为医学开辟了新途径,为创新的微创疗法带来了希望。
过去十年间,制药业界利益相关者、监管机构和医生等对新兴微生物组治疗行业发展的讨论越来越多。这一领域最初引发了一些疑问,此后这些对话不断发展,表明随着时间的推移,人们的态度发生了明显的积极转变。
美国食品及药物管理局(FDA)分别于 2022 年 11 月和 2023 年 4 月批准了两种微生物组产品,为更多微生物组产品在更广泛的适应症上取得进展和监管许可铺平了道路。微生物组疗法带来的潜在益处现已得到广泛认可。
不过,随着基于微生物组疗法的后期临床开发、生产、质量控制流程和监管的发展,标准化成为一项关键而复杂的挑战。微生物的医药产品存在不少复杂性,在临床开发的不同阶段以稳健的方式表征和测量这种复杂性时也会遇到不少新挑战,这些挑战可能会延迟产品的上市进程。
Part 1
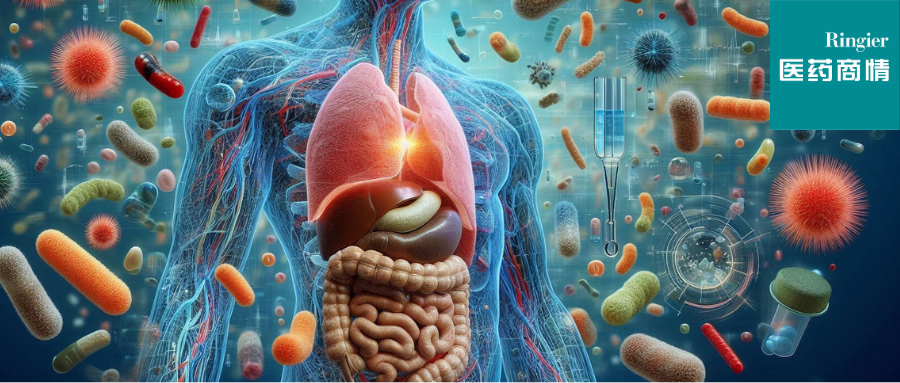
肠道微生物组:一座治疗金矿
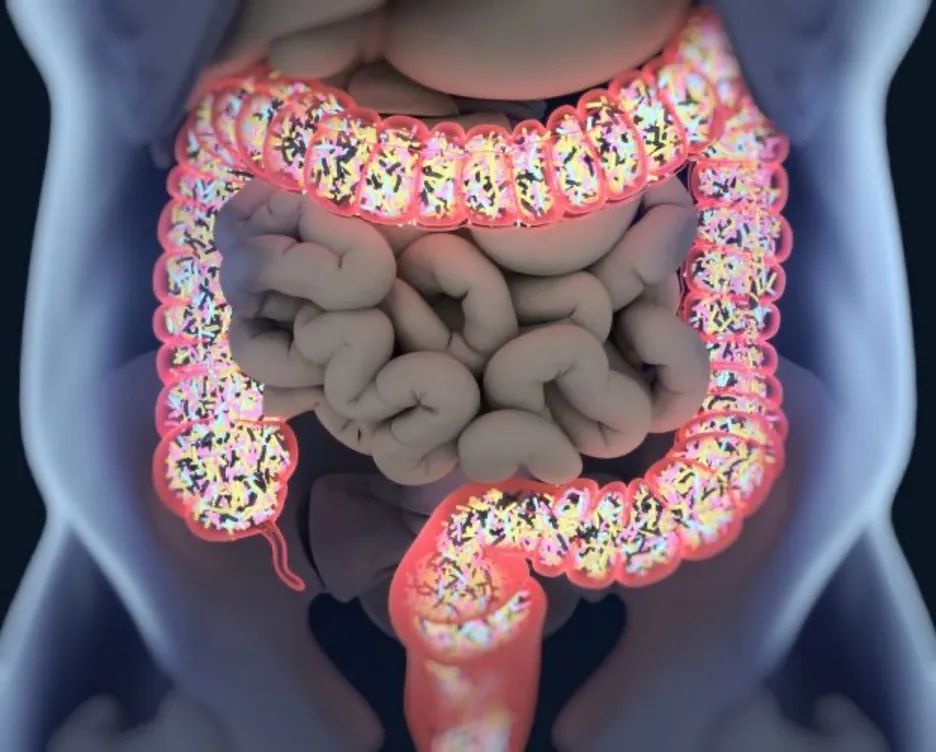
人体肠道是一个充满活力的生态系统,其中有各种各样的细菌、病毒、真菌和其他微生物。这个错综复杂的网络对于维持肠道健康、免疫系统甚至心理健康都至关重要。
肠道问题破坏与多种疾病有关,包括炎症性肠病、癌症、代谢紊乱和神经退行性疾病。人们认识到操纵和利用肠道微生物组治疗和预防疾病的潜力,因此出现了一波临床试验热潮。
然而,随着这一领域的扩展,它也面临着同样日益增多的一系列概念和技术挑战。
Part 2
不同于传统疗法
许多挑战的基础是微生物组的动态性质,而人们对微生物组的探索和了解还远远不够。
微生物组是一个不断变化的生态系统,受饮食、运动、环境和健康状况等变化的影响。必须认识到,微生物组组成和功能的变化并不局限于患有疾病的个体。这种对生态系统的敏感性,加上人体和生活方式的复杂性,使得很难理解微生物组是如何受其环境影响的,以及这些变化是如何影响人体的。
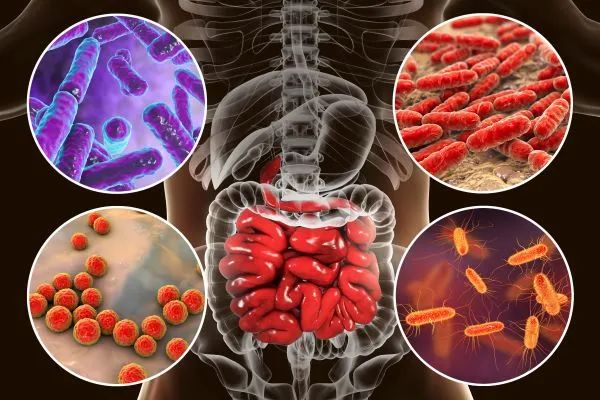
所有微生物组,即使是健康的微生物组,都可能含有致病微生物,但不会引起炎症或感染,如艰难拟梭菌(Clostridium difficil)。
艰难拟梭菌对某些人来说会导致严重感染,但在健康人的微生物组中也发现了艰难拟梭菌,而且没有任何问题。
每种微生物成为致病菌的潜力也可能受环境的影响,甚至导致休眠,而严格基于 DNA 的调查常常忽略了这一点。对微生物组生态学和动态缺乏全面了解会影响创新的各个阶段;从描述作用机制到剂量、毒性、疗效,最终影响临床试验的成功。
扰乱生态系统会导致生物多样性丧失、种群失衡、栖息地破坏、功能改变(如新陈代谢和营养循环)、复原力丧失以及更易感染疾病。操作微生物组需要一定程度的生态系统干扰,而预测和控制这些干预措施对微生物组和人体的影响需要更好地了解人体微生物生态学,这并不是一项简单的任务。
除细菌外,微生物组中还有真菌、古细菌、病毒和寄生虫,这些微生物在生态系统中发挥着作用,但人们对它们的研究和了解并不多。
这种动态的微生物相互作用包括争夺营养、交叉进食和基因交换等,从而导致微生物群组成和功能的波动。
必须强调的是,这些事件的动态过程非常复杂,相互关联,而且每个人的情况也大不相同。
微生物组疗法的开发不同于传统的化学制剂,需要使用活的生物体和复杂的微生物群落。这种独特的作用模式具有潜力和公认的疗效,但鉴于其复杂性,还需要更新整体风险管理方法。
与监管机构的持续对话,有助于设计出符合最新安全标准和国际法规的临床试验。在这一领域开展工作并将微生物群作为一种治疗方法时,重要的是要以全面的视角看待患者,并改善患者的整体健康状况和治疗效果,而不仅仅是提供一种治疗方法。
在使用粪便衍生材料进行临床试验的开发过程中,安全性至关重要。执行严格的规范不仅能保证产品的安全性,还能确保质量和疗效的可重复性。
例如,在收集粪便之前,要对捐献者进行筛查,采集各种血液和粪便样本,检查是否存在多种有害细菌,包括多重耐药菌或致病菌。这些方法也承认有必要适应外部环境的变化,在大流行病开始后成功调整 COVID-19 的筛查就是一例。
在收集粪便时,专家们还会考虑微生物的数量及其潜在的种类和多样性,以了解捐献者个体微生物组的整体健康和功能。
Part 3
人体质量控制:数据可信吗?
技术上的挑战使得将微生物组作为一个生态系统来理解变得更加困难。
虽然全息技术的发展给微生物组研究带来了革命性的变化,但由于这些方法存在固有的偏差,而且缺乏有效的标准化,因此产生的数据受到了影响。从取样、储存到提取和分析,方法各不相同,结果也不尽相同,导致研究结果相互矛盾。
多年来,这种对数据缺乏信心的情况加剧了人们对这一领域的担忧,对于真菌和病毒等研究不足的微生物来说,这一问题变得更加严重。
随着技术的进步,人们开始质疑菌种的分类和定义,以及微生物的功能能力,从根本上考虑基因组结构、表型可塑性、功能冗余和基因表达调控。
Part 4
标准化势在必行
微生物组疗法的复杂性和潜在变异性要求——在研究和开发的各个阶段实现强有力的标准化。
微生物组疗法的标准化工作已在进行中,目前已有一些参考试剂,国际研究也揭示了世界各地方法的差异性。这些标准应健全并适用于不断发展的领域,适应微生物组科学和技术的进步。
标准化方法的好处包括:数据可信度高,可为临床试验提供更可靠的疗效证据;可靠的证据可减少监管机构的不确定性,加快审批速度,最终加快患者获得这些治疗方法的速度;确保疗法始终符合质量和安全标准,保护受试者免受潜在伤害和/或不可靠疗法的影响;培养对行业的信任,吸引投资,促进创新。
Part 5
池化或成“下一代”解决方案
每个人的肠道微生物组都是复杂而独特的,由微生物的不同组成和每个微生物组固有的个性所决定。
值得注意的是,不同的供体之间存在显著差异。虽然这种方法对艰难梭菌的治疗安全有效,但供体之间的差异可能会导致免疫介导疾病患者的随机结果和反应。
因此,了解并解决个体肠道微生物组的复杂性对于确保基于微生物组的疗法的安全性和可靠性至关重要。
对此,一家法国生物技术初创公司MaaT Pharma 开发了一种池化(pooling)过程技术并申请了专利,该技术被认为是解决不同供体肠道微生物组差异的战略性解决方案。
研究表明,将来自多个供体的粪便提取物结合起来,可以获得更多样化的产品,提供患者所需的全部微生物。池化还具有以下潜力,如使产品成分标准化,显著减少汇集产品的差异;在危及生命的适应症中有效恢复微生物组的平衡,例如治疗血癌的造血干细胞移植后的严重并发症移植物抗宿主病(GvHD)。
Part 6
推进微生物组创新
微生物组疗法的未来将以艰难梭菌感染之外的多种疾病领域,尤其是肿瘤领域的新疗法的发展为标志。例如,许多研究都强调了肠道微生物组在提高化疗药物疗效和降低其毒性方面的作用。
值得注意的是,微生物组疗法在肿瘤血液学中具有强大的潜力,抗生素和化疗导致的肠道多样性丧失可预测接受异基因造血干细胞移植患者的死亡率,以及 GvHD 发生率和感染率。
据了解,MaaT Pharma的候选药物 MaaT033 就利用了微生物组疗法,目前正在欧洲的一项 II 期试验中对接受异基因造血干细胞移植的患者进行评估。
对于GvHD和早期治疗失败的患者,微生物组疗法可以通过恢复肠道微生物组生态系统,帮助维持患者的免疫功能,而不过分损害其免疫功能,从而降低感染并发症和复发的风险,从而引入一种新的治疗方法。这可以提供一种独特的免疫恢复选择,作为标准免疫抑制药物的补充,对于没有治疗选择的患者来说,这可能是一个潜在的突破。
此外,最近的研究开始更广泛地揭示肠道微生物群的作用,并将异常与肌萎缩性脊髓侧索硬化症(ALS)等疾病联系起来。肠道微生物群与渐冻症之间的联系首先来自临床前证据,然后来自临床观察,表明肠道微生物群对疾病有调节作用。
Part 7
临床试验:确保安全有效的疗法
微生物组疗法的后期临床开发涉及设计和开展稳健的临床试验。
然而,人类微生物组在个体、健康状况甚至时间上的多样性使试验设计和数据解读变得更加复杂。此外,由于物种间可转移疾病表型的过度报告以及所产生的数据与人类健康的相关性,围绕临床前试验数据的审查日益增多。
创新者必须解决如何全面评估产品的质量和一致性问题,他们有责任证明并建立报告程序来实现这一目标。
事实证明,微生物组,甚至微生物相关微粒,都可能引起不同的免疫反应和毒性,因人而异。因此,必须采用基于风险的方法并考虑目标人群,严格控制剂量。
归根结底,由于微生物群的特性,临床试验的结果可能会不尽相同,但必须相信数据是真实、准确和可靠的,同时努力了解变异的来源,以便将产品推向市场。
为了应对这些挑战,研究界必须通力合作,制定出一致认可的标准,例如纳入和排除标准,以及控制和/或考虑共源因素和使用标准化报告的标准。此外,与监管机构进行开诚布公的讨论至关重要,这将有助于确保临床试验结果的可解释性和可信度。
Part 8
加速微生物组疗法的普及
新药从研发到上市一般要经历4至6年甚至更长时间的临床前及临床研究。
一些特殊疾病、重症疾病患者往往由于等不到药品上市、不符合临床试验纳入标准或者被分配到对照组而延误治疗,为此,“同情用药(compassionate use)”应运而生。
一些欧美国家有一类制度或者计划与同情用药制度类似,统称为早期准入计划(early access programs,EAP),在符合特定标准,按照特定条款的前提下,向特定患者提供未取得上市许可药品的一项特殊国家监管制度。
例如美国的同情用药(CU)和扩展使用(EA)、欧盟的患者用药计划(named patient programme,NPP)和优先药物(priority medicines,PRIME)计划、英国的早期获取药物计划(early access to medicines scheme,EAMS)、加拿大的特殊获取计划(special access program,SAP)、澳大利亚的授权处方方案(authorized prescriber scheme,APS)和特殊获取方案(special access scheme,SAS)等。
EAP 在推动微生物组疗法的发展和促进其潜在未来方面发挥着至关重要的作用,它提供了一条解决未满足医疗需求的途径,为那些可能不符合传统临床试验条件的患者以及那些无法承受传统药物开发漫长过程的患者提供了潜在的解决方案。
EAP 的意义还在于它能够利用真实世界的数据,深入了解新兴疗法的有效性和安全性。
虽然临床试验可以在受控环境下为医疗产品的安全性和有效性提供证据,但对于新药在现实世界中的表现,往往缺乏重要的数据。
因此,应将 EAP 视为临床试验的重要补充,使制药公司能够更好地了解患者在受控临床环境之外对治疗的反应。这可以涉及更广泛的患者,包括具有不同健康状况和病史的患者,从而更全面地了解治疗反应以及疗效和安全性方面的潜在差异。
例如,最近欧洲一项 MaaT Pharma 使用池化供体微生物组生态系统疗法 MaaT013 的 EAP 结果表明,该疗法是安全的,而且难治性急性 GvHD 患者的胃肠道总反应率(GI-ORR)很高,第 28 天为 54%。阳性反应对总生存率有很大影响,尤其是对目前治疗无效的患者,有反应者为67%,无反应者为24%。在皮质类固醇和Ruxolitinib治疗失败后,将MaaT013作为第三线治疗,28天时的消化道ORR为61%,应答者为81%,非应答者为8%。
微生物组具有巨大的治疗潜力,为治疗和预防多种疾病带来了新希望。然而,后期临床开发、生产、监管和质量控制等方面的挑战要求行业齐心协力,加快这一领域的创新。
标准化不是一种选择,而是势在必行。只有建立明确的、国际公认的标准,才能确保微生物组疗法的安全、有效和一致发展。研究人员、制造商、监管机构和临床医生的共同努力将为微生物组疗法的未来奠定基础,充分释放这一令人兴奋的领域的潜力,造福全球患者。
Part 9
微生物组疗法:一个新时代
微生物组领域为我们治疗疾病提供了一种令人振奋的新方法。
将重点从免疫抑制转移到免疫恢复是一种新的作用模式,与传统方法相比,它有可能减少感染和并发症,并为从代谢性疾病到神经系统疾病和炎症性疾病等一系列往往被忽视的严重疾病提供突破性的治疗方案。
为了充分发掘微生物组的潜力,需要回归最基本的认知,将微生物组视为一个复杂而动态的生态系统。微生物组创新者应打破常规思维,直面挑战,承认当前方法的先天局限性,从而为微生物组创新铺平道路。世界各地的监管机构都意识到了这些挑战,并越来越多地鼓励在申请过程的最初阶段进行积极讨论。任何新兴研究领域都会面临挑战,但变革性进展的潜力给我们带来了希望,让我们对微生物组疗法的未来保持好奇和乐观。
参考文献
1. US FDA approves Ferring’s Rebyota for Clostridioides difficile infection. [Internet] Pharmaceutical Technology. 2022. [cited 2024Feb]. Available from: https://www.pharmaceutical-technology.com/news/fda-ferring-rebyota-cdi/
2. FDA Approves First Orally Administered Fecal Microbiota Product for the Prevention of Recurrence of Clostridioides difficile Infection 2024. [cited 2024Feb]. Available from: https://www.fda.gov/news-events/press-announcements/fda-approves-first-orally-administered-fecal-microbiota-product-prevention-recurrence-clostridioides
3. Malard F, Loschi M, Huynh A, et al. Pooled Allogeneic Faecal Microbiota MAAT013 For Steroid-Resistant Gastrointestinal Acute Graft-Versus-Host Disease: A Single-Arm, Multicentre Phase II trial. eClinicalMedicine. 2023; 62:102111.
4. Oh B, Boyle F, Pavlakis N, et al. Emerging Evidence Of The Gut Microbiome In Chemotherapy: A Clinical Review. Front. Oncol. 2021;11.
5. Peled JU, Hanash AM, Jenq RR. Role of The Intestinal Mucosa In Acute Gastrointestinal GVHD. Blood. 2016;128(20):2395–402; Staffas A, Burgos da Silva M, van den Brink MR. The Intestinal Microbiota In Allogeneic Hematopoietic Cell Transplant And Graft-Versus-Host Disease. Blood. 2017;129(8):927–33; Taur Y, et al. The Effects Of Intestinal Tract Bacterial Diversity On Mortality Following Allogeneic Hematopoietic Stem Cell Transplantation. Blood. 2014;124(7):1174-82; Jenq RR, Taur Y, Devlin SM, et al. M. Intestinal Blautia Is Associated With Reduced Death From Graft-Versus-Host Disease. Biol. Blood and Marrow Transplantation. 2015;21(8):1373–83.
6. Kamada N, Kim YG , Sham HP, et al. Regulated Virulence Controls the Ability of a Pathogen to Compete with the Gut Microbiota. Science [Internet]. 2012. [cited 2023 Dec];336(6086):1325–9. Available from: https://science.sciencemag.org/content/336/6086/1325.long
7. A Landscape of Opportunities for Microbial Ecology Research [Internet]. 2020. frontiersin.org. [cited 2023 Dec] Available from: https://www.frontiersin.org/articles/10.3389/fmicb.2020.561427/full
8. Nearing JT, Comeau AM, Langille MGI. Identifying biases and their potential solutions in human microbiome studies. Microbiome. 2021 May 18;9(1).
9. Van Rossum T, Ferretti P, Maistrenko OM, Bork P. Diversity within species: interpreting strains in microbiomes. Nature Reviews Microbiology [Internet]. 2020 [cited 2023 Dec] 4;1–16. Available from: https://www.nature.com/articles/s41579-020-0368-1
10. WHO/BS/2022.2416: A WHO collaborative study to evaluate the candidate 1st WHO International Reference Reagents for Gut Microbiome analysis by Next-Generation Sequencing [Internet]. www.who.int. [cited 2023Dec]. Available from: https://www.who.int/publications/m/item/who-bs-2022.2416
11. WHO/BS/2023.2455 WHO 1st Reference Reagent for DNA extraction of gut microbiome [Internet]. www.who.int. [cited 2023Dec]. Available from: https://www.who.int/publications/m/item/who-bs-2023.2455