荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
在当今日新月异的美容科技领域中,外泌体作为一种纳米级生物活性载体,正逐渐改变化妆品和个护产品的创新轨迹。近期一篇发表于《Cosmetics》期刊的一篇重要综述论文「Use of Exosomes for Cosmetics Applications」系统性地阐述了外泌体在化妆品领域的应用前景,由墨西哥巴哈加利福尼亚自治大学的 Luis Jesús Villarreal-Gómez 教授等专家组成的研究团队所完成的综述,为我们揭示了这一微小却功能强大的细胞衍生物如何影响着美容个护产业。

外泌体研究的爆发式增长
外泌体是由细胞分泌的膜包被小泡,作为细胞间通讯的“信使”,它们携带着调控细胞功能的生物活性分子。这些直径仅为 30-150 纳米的细胞分泌物,携带着蛋白质、脂质和核酸等生物活性物质,在细胞间传递信息,扮演着“生物信使”的角色。不少研究表明,外泌体能够影响受体细胞的基因表达和蛋白质合成,从而调节多种生物学过程,包括免疫应答、组织修复和再生。
根据该综述文章的分析结果,过去十年间,外泌体研究领域呈现爆发式增长,相关论文数量从 2014 年的 918 篇飙升至 2024 年的 5382 篇,增长幅度超过 430%。研究团队通过分析 36173 篇发表于 2014 至 2024 年这十年间的论文发现,外泌体在化妆品领域的应用研究中,伤口愈合相关研究最为丰富(1438篇),其次是生物分子递送(187篇)和抗衰老(62篇),而皮肤保湿研究仅有 7 篇,表明存在巨大的研究空白与发展潜力。
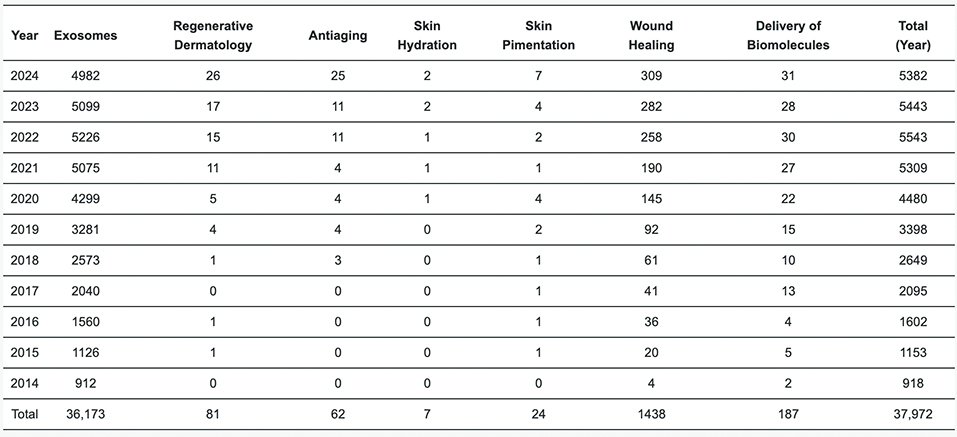
表1. 2014-2024 年发表的与外泌体和外泌体在化妆品中的应用有关的期刊文章
外泌体的组成与提取工艺
研究团队在综述中详细描述了外泌体的提取和制备工艺。这种纳米级囊泡可通过超速离心技术从多种细胞培养物中获取,包括来自脂肪组织活检的间充质干细胞(MSCs)、角质形成细胞或脂肪细胞。提取后的外泌体经冻干处理,可直接使用或与其他分子载体结合,用于化妆品配方中。典型的外泌体包含多种生物活性成分,其中最引人注目的是生长因子。
研究显示,表皮生长因子(EGF)、成纤维细胞生长因子(FGF)和转化生长因子-β(TGF-β)等共同增强了皮肤再生和抗衰老效果,激活细胞更新并促进细胞外基质重塑。研究团队特别强调,外泌体的组成非常复杂,除了生长因子外,还包含热休克蛋白、细胞因子和信号分子,这些成分协同作用,为皮肤健康和修复提供全方位支持。
外泌体在美容个护领域的应用
. 皮肤再生与抗衰老
外泌体在皮肤再生和抗衰老领域表现出卓越功效。研究团队引用了 Chen 等人的研究,证明了从脂肪组织干细胞分离的外泌体能显著改善脂肪移植物的保留率(达56.4%±1.6%),远高于对照组。这种组织再生能力在皮肤抗衰老应用中具有重要意义。
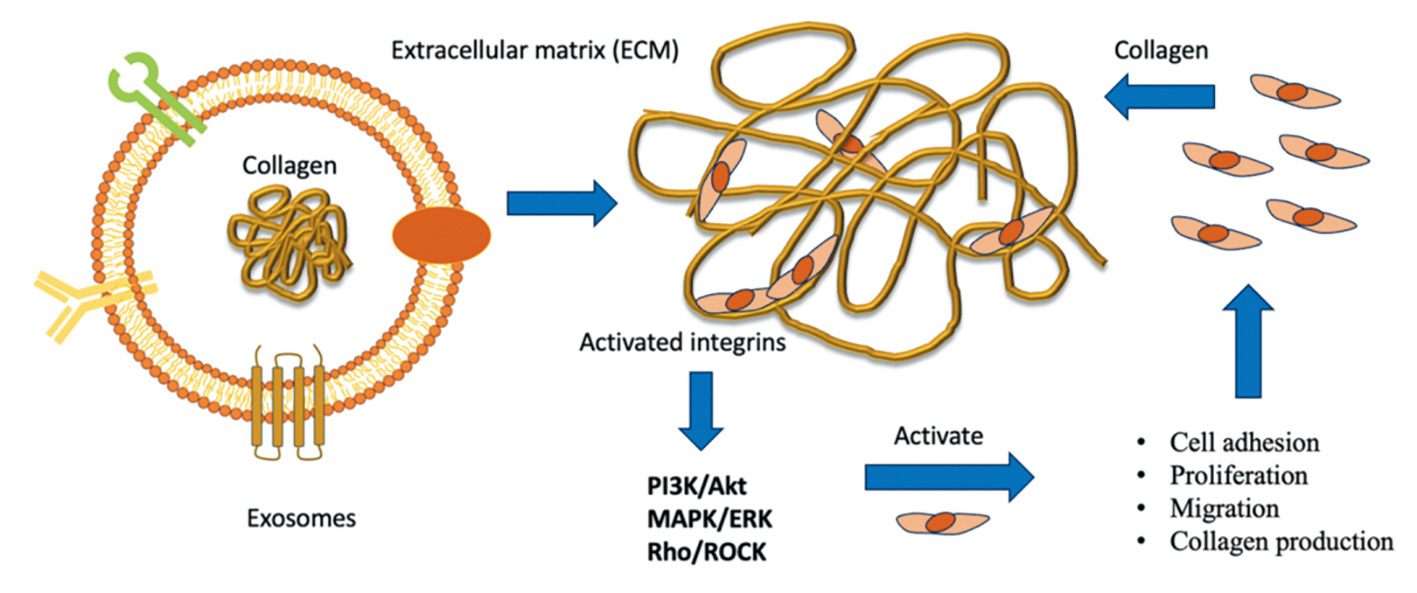
外泌体通过多重机制协同作用,有效延缓皮肤衰老迹象。它们激活成纤维细胞,促进 I 型和 III 型胶原蛋白合成,为皮肤提供支撑结构;同时平衡基质金属蛋白酶(MMPs)的活性,维持胶原蛋白生成与降解的动态平衡。外泌体的抗氧化特性可减少自由基对细胞 DNA 的损伤,起到保护作用,此外还能提高细胞能量利用效率和代谢活性,从根本上改善细胞健康状态。综述引用的临床数据表明,外泌体处理后,皮肤厚度增加 19.3%,皱纹减少 23.6%,弹性增加 31.4%,使用 4-8 周后效果尤为明显。
研究团队在综述中展示了外泌体在皮肤保湿领域的创新应用。虽然相关研究数量有限(仅有 7 篇),但初步结果令人瞩目。外泌体通过增强皮肤屏障功能、减少经皮水分流失(TEWL)、促进透明质酸合成以及改善细胞外基质来提升皮肤保湿状态。
论文引用的 Bahr 等人研究指出,为使外泌体技术在临床上可行,需要制备足量活性外泌体并建立有效的长期保存方法。冷冻保存是目前最常用的方法,但科学家正在探索冻干和室温保存的新技术,这将大大降低外泌体在化妆品中的应用成本。
在所有外泌体来源中,间充质干细胞(尤其是脂肪来源的 ADSC-Exos 和骨髓来源的 BMSC-Exos)表现出最佳的保湿效果。这些外泌体富含生长因子、细胞因子和 microRNA,能刺激真皮成纤维细胞产生透明质酸和胶原蛋白,同时改善皮肤屏障完整性。临床试验数据显示,使用外泌体产品四周后,皮肤水分含量平均提高了 32%,表皮屏障功能改善了 27%。
研究团队特别关注了外泌体在皮肤色素调节方面的双向作用,综述分析了外泌体如何既能治疗色素沉着过度(如黄褐斑),又能帮助色素缺失(如白癜风)的情况,展示了其多功能性。
在治疗黄褐斑方面,外泌体通过抑制酪氨酸酶活性减少黑色素合成,调节小眼畸形转录因子(MITF)信号通路降低黑色素细胞活性,同时发挥抗炎和抗氧化作用,减轻 UV 辐射造成的氧化应激。研究团队引用的一项临床试验显示,使用含 MSC 外泌体的乳霜 8 周后,色素沉着斑点减少 47%,肤色均匀度提高 38%。
有趣的是,角质形成细胞和成纤维细胞衍生的外泌体在色素调节中表现出不同的作用机制。角质形成细胞衍生的外泌体能转移前列腺素 E2(PGE2)和特定 microRNA 促进黑色素生成,而成纤维细胞衍生的外泌体则通过生长因子和细胞因子调节黑色素生成过程。这种差异为开发针对不同色素问题的定制化产品提供了科学基础。
在所有外泌体化妆品应用中,伤口愈合领域的研究最为丰富,已有 1438 篇相关论文。研究团队详细分析了外泌体如何通过促进血管新生、细胞增殖和胶原重塑加速伤口愈合过程。

Prasai 等研究者的分析涵盖了 51 项啮齿动物研究,发现外泌体的治疗效果在给药后第 7 天最为显著(优势比 1.82,95% 置信区间 [0.69, 2.95])。外泌体通过 microRNA 的作用调节皮肤伤口愈合的各个阶段,从初始炎症反应到最终的组织重塑。
Zhao 等研究人员的发现进一步证实了间充质干细胞衍生的外泌体是促进组织再生的关键因素。这些微小囊泡能够刺激血管新生、促进细胞增殖、提高胶原蛋白产生,调节炎症反应,最终增强组织修复能力。研究团队特别指出,这一发现对化妆品行业具有深远意义,尤其是在疤痕修复和创伤后皮肤护理产品开发方面。
临床前研究表明,含有外泌体的伤口敷料可使伤口闭合速度提高 40%,瘢痕形成减少 35%,与传统治疗相比具有显著优势。这些数据为外泌体在术后护理和日常微创修复产品中的应用提供了有力支持。
. 高效生物分子递送系统
传统化妆品成分难以穿透皮肤屏障,而外泌体天然的膜结构和细胞亲和性使其成为理想的活性成分载体。
外泌体递送系统的卓越性体现在多个方面——它们具有极高的生物相容性,作为细胞衍生物,极少引起不良反应;其靶向性能够被工程化改造,以针对特定皮肤细胞类型;携带的活性成分受到膜结构保护,避免降解;穿透能力强,可克服皮肤角质层屏障;此外,外泌体可从患者自身细胞分离并定制,开辟了个性化护肤的新途径。
综述引用的最新研究展示了科学家们正在开发的外泌体装载技术,将抗氧化剂、多肽、透明质酸等活性成分精准装载于外泌体中,以提高其生物利用度和靶向性。
. 个性化护肤
综述论文结尾部分特别展望了外泌体开启的个性化护肤的可能性,通过从特定细胞源分离或调节外泌体携带特定生物活性分子,可为不同肤质和肌肤问题提供真正的定制化解决方案。
Frazier 等人的研究指出,由脂肪组织、血液和纤维素衍生的产品,包括细胞、去细胞基质和支架,以及外泌体和分泌因子,有望满足个性化医疗美容需求。具体应用场景包括抗衰老、敏感肌修复、美白均肤和毛孔问题等。
临床研究数据显示,个性化外泌体护肤方案较标准化护肤方案效果更佳,用户满意度提高 64%,效果感知提升 78%。
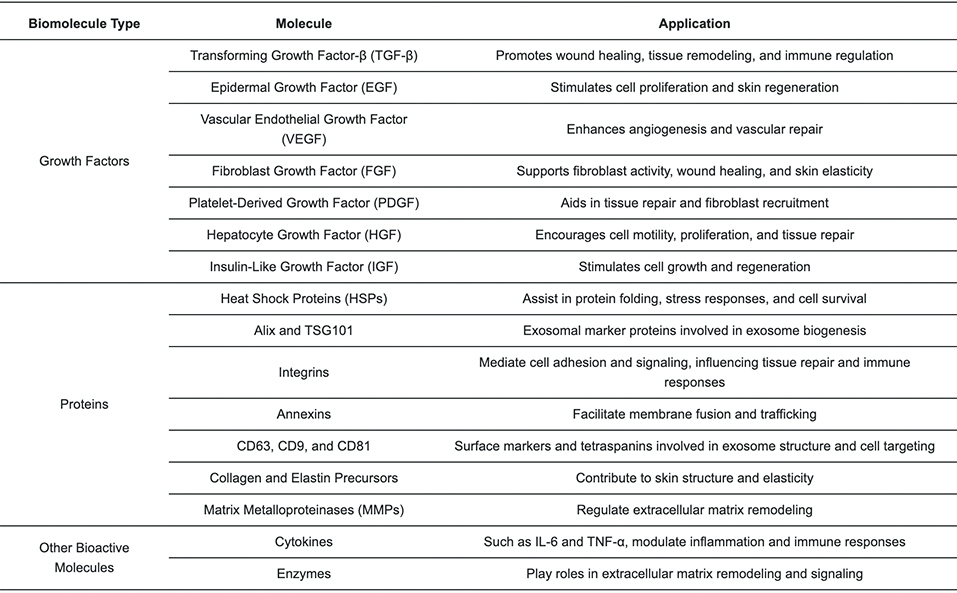
表 2. 外泌体的生物大分子组成及其主要
. 外泌体应用的挑战与未来展望
尽管外泌体在化妆品领域展现出巨大潜力,但研究团队也坦率指出了当前面临的严峻挑战。
首先是标准化生产问题——外泌体质量因细胞来源、分离方法和存储条件而异,难以保证批次间一致性。此外,高纯度外泌体的大规模生产仍面临技术障碍,制约了其商业化进程。
其次,临床验证仍不充分,大多数研究集中在体外或动物模型,人体临床试验样本量小且周期短。
监管挑战也不容忽视,FDA 和 EMA 等监管机构尚未为外泌体化妆品制定全面指南。Ku 等人的研究指出,尽管外泌体在医学美容领域日益受到关注,但截至目前尚无外泌体产品获得 FDA 批准。部分制造商虽然声称产品处于“待批准”状态,但实际上还需要更多临床研究来确立外泌体在美容整形和化妆品中的安全性及有效性。
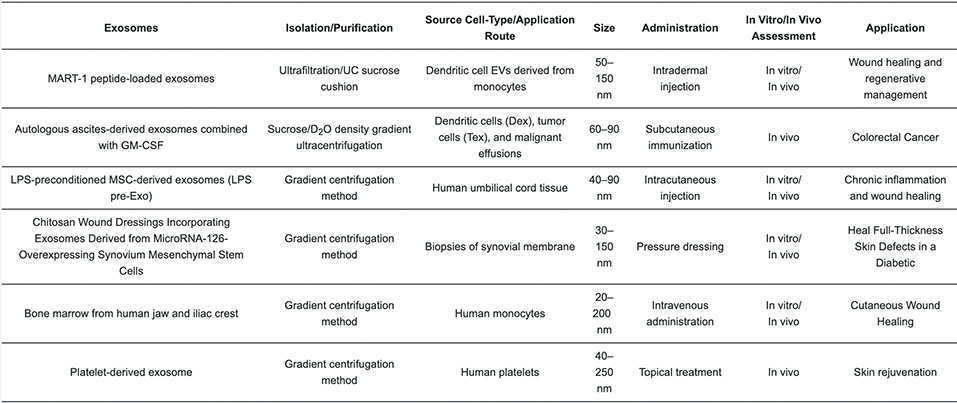
表 3. 外泌体的一些生物医学应用
伦理问题是外泌体应用中不可回避的另一挑战。人源外泌体引发了相当的伦理争议,可能会限制某些外泌体产品的广泛接受度。
尽管面临这些挑战,研究团队仍对外泌体技术的未来持乐观态度。综述预测了几个可能的发展趋势——
工程化外泌体技术将进一步完善,使科学家能更精确地定制外泌体载荷,靶向特定皮肤问题;植物源外泌体的开发有望解决伦理和监管问题;结合水凝胶、纳米纤维等新型材料可提高外泌体的稳定性和渗透性;外泌体与传统活性成分的协同应用将创造出效果更佳的组合疗法;便携式外泌体提取技术的发展可能推动即时个性化护肤方案等。
参考文献:
[1] 1. Villarreal-Gómez, L. J., Origel-Lucio, S., Hernández-Hernández, D. A., & Pérez-González, G. L. (2025). Use of Exosomes for Cosmetics Applications. Cosmetics, 12(1), 9.
[2] Chen, B., Cai, J., Wei, Y., Jiang, Z., Desjardins, H. E., Adams, A. E., Li, S., Kao, H.-K., & Guo, L. (2019). Exosomes are comparable to source adipose stem cells in fat graft retention with up-regulating early inflammation and angiogenesis. Plastic and Reconstructive Surgery, 144(5), 816e-827e.
[3] Bahr, M. M., Amer, M. S., Abo-El-Sooud, K., Abdallah, A. N., & El-Tookhy, O. S. (2020). Preservation techniques of stem cells extracellular vesicles: A gate for manufacturing of clinical grade therapeutic extracellular vesicles and long-term clinical trials. International Journal of Veterinary Science and Medicine, 8(1), 1-8.
[4] Prasai, A., Jay, J. W., Jupiter, D., Wolf, S. E., & El Ayadi, A. (2022). Role of exosomes in dermal wound healing: A systematic review. Journal of Investigative Dermatology, 142(3), 662-678.e8.
[5] Zhao, H., Li, Z., Wang, Y., Zhou, K., Li, H., Bi, S., Wang, Y., Wu, W., Huang, Y., Peng, B., Yuan, L., Zeng, Z., & Kuang, S. (2023). Bioengineered MSC-derived exosomes in skin wound repair and regeneration. Frontiers in Cell and Developmental Biology, 11, 1029671.
[6] Frazier, T., Alarcon, A., Wu, X., Mohiuddin, O. A., Motherwell, J. M., Carlsson, A. H., Christy, R. J., Edwards, J. V., Mackin, R. T., Prevost, N., Ghali, S., & Bowlin, G. L. (2020). Clinical translational potential in skin wound regeneration for adipose-derived, blood-derived, and cellulose materials: Cells, exosomes, and hydrogels. Biomolecules, 10(10), 1373.
[7] Ku, Y. C., Omer Sulaiman, H., Anderson, S. R., & Abtahi, A. R. (2023). The potential role of exosomes in aesthetic plastic surgery: A review of current literature. Plastic and Reconstructive Surgery - Global Open, 11(4), e5051.
来源:荣格-《 国际个人护理品生产商情》
原创声明:
本站所有原创内容未经允许,禁止任何网站、微信公众号等平台等机构转载、摘抄,否则荣格工业传媒保留追责权利。任何此前未经允许,已经转载本站原创文章的平台,请立即删除相关文章。

