荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
今年CRISPR研究界的期望很高,因为全球首个基于此技术的疗法即将获得美国FDA的批准。CRlSPR基因编辑长期以来吸引了研究界、媒体和广大公众的关注,在2020年达到了顶峰,当时瑞典皇家科学院将诺贝尔化学奖授予了两位领先的CRISPR研究人员Jennifer Doudna和Emmanuelle Charpentier。然而,该领域也面临着不少争议。
一些基因疗法虽然通过增加修改过的基因的功能拷贝来纠正缺陷,但是通过CRISPR(即聚类规律性间隔短链重复序列)进行的基因编辑,可以针对并修改特定的DNA序列。引导RNA将Cas9酶引向目标DNA序列,该序列可以被编辑成所需的变化。重要的是,CRISPR编辑比其他方法更容易获得,使基于CRISPR的研究更容易、更平价。
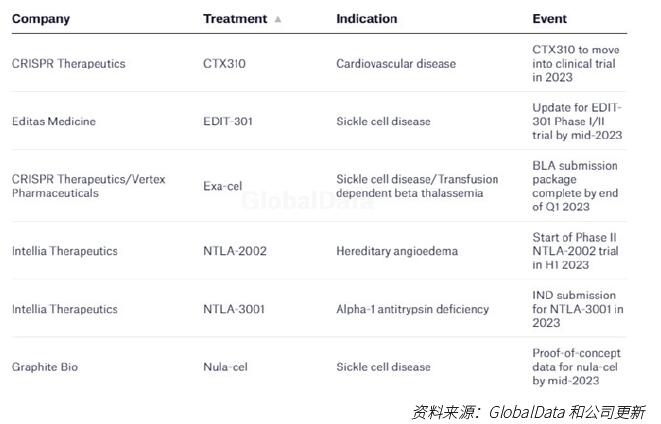
尽管如此,目前还没有使用这此技术的治疗方法获得批准。不过情况可能很快就会不同——2022年美国血液学会(ASH)年会上,展示了一些正在开发的用于治疗血液疾病的最先进的基于CRISPR的疗法。其中,由CRISPR Therapeutics和Vertex Pharmaceuticals公司制造的基因疗法exagamglogene autotemcel,也被称为exa-cel,成为最接近潜在批准的疗法。这两家公司都计划在获得积极数据后,于2023年第一季度结束前完成该疗法的BLA申请,用于治疗镰状细胞病(SCD)和输血依赖性β地中海贫血(TDT)。
exa-cel等疗法的临床成功,正在使基于CRISPR的治疗潜力越来越接近患者。“这种势头是真实存在的,2021年很好,2022年更好。” 罗利的北卡罗来纳州立大学益生菌研究领域的Todd R. Klaenhammer特聘教授Rodolphe Barrangou博士表示说道。Barrangou是位于马萨诸塞州剑桥市的Intellia Therapeutics公司的联合创始人,该公司是CRISPR基因疗法的开发商,他仍是该公司科学委员会的成员。他表示,在2023年,在不同适应症和下一代基因疗法患者的第一阶段试验中继续测试这一疗法将是非常重要的。
首次批准将是CRISPR疗法的一个里程碑,一些专家也强调,该行业正在取得进展,今年对于建立CRISPR基因编辑的监管先例至关重要,一对该领域的进一步发展至关重要。
血液病的治疗方法处于领先地位
哥本哈根大学蛋白质结构与功能项目研究主任Guillermo Montoya博士表示,基于CRISPR的血液病治疗试验在2022年特别成功,例如SCD。
马萨诸塞州波士顿大学Chobanian & Avedisian医学院医学教授Martin Steinberg博士表示,exa-cel的临床成功代表了某种里程碑,“就在不久之前,人们还难以置信地认为,可以围绕一个主要被抑制的基因的表达做到这样,而这将导致看起来是一种治愈或接近治愈的效果。”
根据去年ASH会议上分享的SCD II/III期CLIMB SCD-121试验的结果,所有31名接受治疗的患者都没有出现血管闭塞危机。从输注exa-cel到最后一次输红细胞的中位时间是19天。
exa-cel并不是唯一吸引该领域专家注意力的临床开发产品。Intellia Therapeutics公司和诺华公司正在开发的SCD疗法OTQ923正处于I/II期研究。田纳西州孟菲斯圣裘德儿童医院的研究助理、该试验的调查员Akshay Sharma博士表示,根据一项研究的初步结果,两名接受OTQ923治疗的患者的胎儿血红蛋白水平得到了改善,因此有必要进一步研究。
预计到2023年,将有更多药企带来消息。Editas Medicine的目标是在2023年中期获得I/II期RUBY试验的临床更新,该试验测试CRISPR-Cas12a疗法EDIT-301在SCD中的应用。Intellia计划在今年某个时候提交NTLA-3001的申请,一种CRISPR介导的治疗α-1抗胰蛋白酶缺乏症的疗法,Intellia还计划在2023年上半年开始NTLA-2002的二期研究,一种治疗遗传性血管性水肿的CRISPR疗法。此外,Graphite Bio预计在2023年中期对其SCD疗法nula-cel进行I/II期研究,获得概念验证数据。Nula-cel是UltraHDR平台的一部分,Graphite Bio将其描述为下一代的基因编辑。
建立监管框架非常重要
然而,在取得临床进展的同时,Barrangou也强调,这一领域的进展不应简化为对批准和失败的二元理解,解决CRISPR研究的监管问题是今年需要关注的主要挑战之一。
“我认为必须看到在美国提交 IND 申请的增加,并得到令人信服的支持,FDA 必须增强紧迫感,并与其中一些公司合作,保持这种势头向前推进。对于一些分析师、监管机构和企业来说,还有待了解。”
批准之后,基于CRISPR的疗法的定价框架也需要建立。Sharma指出,Exa-cel的潜在价格将非常重要,特别是在bluebird bio的潜在竞争背景下。bluebird bio获批的TDT基因疗法Zynteglo在美国的价格为280万美元,此前曾面临定价问题。Zynteglo不是基于CRISPR的疗法,而是使用慢病毒载体将β-球蛋白的工作拷贝加入患者的造血干细胞中。
需要更多工作
Montoya表示,未来几个月的重点将是进一步加强CRISPR临床试验的数量。他解释说,在不同疾病的临床试验中测试基于CRISPR的疗法将表明该技术可以是安全的。他指出,这然后可以为测试更复杂的疾病的治疗提供信心。
2022年11月,美国生物技术公司Verve Therapeutics宣布,其治疗方法VERVE-101在杂合子家族性高胆固醇血症(HeFH)的潜在一期试验的IND申请被FDA搁置了。FDA要求提供关于种系编辑的风险以及人类和非人类细胞之间效力差异的进一步临床前数据。然而,这种疗法的I期心脏-1试验仍在新西兰和英国进行。
伦敦大学学院皇后广场神经学研究所临床与实验癫痫学副教授Gabriele Lignani博士表示,在癫痫等其他情况下,研究人员正试图了解潜在的CRISPR系统的功效,即有多少神经元可以受到治疗的影响。他说,鉴于脑部疾病的复杂性,基于CRISPR的治疗方法的影响程度仍然未知。
Lignani的研究包括研究CRISPR系统如何用于治疗遗传疾病,如Dravet综合症。这一领域的下一个里程碑将是进行长期的毒性研究,特别是在大型动物身上。据Lignani表示,基于CRISPR的大脑治疗的一个大挑战是免疫系统对Cas9表达的反应。
为这些复杂的适应症开发CRISPR疗法仍然是一个长期目标。Montoya表示,开发新的方法和技术来针对涉及多个基因的复杂疾病将是下一个前沿领域,可能是我们未来必须解决的剩余和长期的挑战之一。
作者:Adam Zamecnik
来源:Pharmaceutical Technology
来源:荣格-《国际医药商情》
原创声明:
本站所有原创内容未经允许,禁止任何网站、微信公众号等平台等机构转载、摘抄,否则荣格工业传媒保留追责权利。任何此前未经允许,已经转载本站原创文章的平台,请立即删除相关文章。