荣格工业资源APP
了解工业圈,从荣格工业资源APP开始。
面向口服配制小分子原料药,往往面临溶解性(solubility)差的问题。溶解性对非消化道给药产品也很重要。注射剂产品需要不含颗粒(外来物质和活性成分),而且往往是高浓度配方,如果药物物质的水溶性较差,这两点就很难实现。特殊辅料可以帮助克服这些溶解性问题。候选辅料包括聚合物胶束和脂质基配方。
药物开发中的常见问题:溶解性差
溶解性是大多数新发现的候选药物所面临的挑战,无论其递送途径如何。事实上,市场上大约40%的原料药和大约90%的开发中的原料药水溶性很差。如今,以目标为导向的高通量筛选,旨在识别更多的亲脂性化合物,再加上更大、更复杂的分子的趋势,都有助于开发出溶解度更低的原料药。
在药物开发过程中,许多分子目标,如药物/酶结合点,都是疏水性的。由于同类相吸,候选原料药的主要结构也往往是疏水性的,使它们在水介质中的溶解度很低。
分子量、化学结构和化学组亲油性是影响小分子原料药溶解度的关键因素。一些以肽为基础的药物也会因其氨基酸组成而导致溶解度低下,而蛋白质也有溶解度的挑战。就肽和蛋白质而言,当这些分子的三级结构在表面包括大量疏水部分,从而暴露在水介质中时,通常会出现溶解度差的情况。通常可以通过进行pH值或离子强度研究来规避,以找到蛋白质结构包含暴露的带电部分的正确窗口。
高药物负荷
溶解性不仅对口服药物很重要,对非消化道给药制剂也很重要,因为这些产品溶液必须是无颗粒。即使是高浓度的产品也必须做到这一点,这是一个不断增长的配方趋势,进一步增加了对高溶解度的需求。
有几种策略用于提高疏水性化合物的溶解度,每种策略都有其局限性。安全性始终是配制新型治疗药物的关键问题,但对于绕过胃肠道并通过血液直接输送到受体部位的非消化道给药制剂来说,安全性就更加关键了。因此,并非所有的策略都是实用的,特别是当配方师试图实现高药物负荷时,例如减少给药频率。水基非消化道给药制剂还必须有合适的补液水平,以避免用药后疼痛的发生。
这一要求限制了目前被美国FDA批准并报告为普遍认为安全(GRAS)的辅料数量。在亲脂性介质中利用油基溶液的非标准配方提出了一套完全不同的问题。
辅料必须提供屏蔽效应
绕过血脑屏障的非消化道给药制剂还意味着这些制剂中使用的辅料必须满足生物负荷、内毒素水平等方面的高质量要求。并非所有可能增加溶解度的辅料都适合用于非消化道给药。
此外,由于许多非消化道给药制剂都是高浓度产品,在使用有限的赋形剂的情况下提高溶解度存在挑战,对于每个特定的API,赋形剂或赋形剂混合物的亲水性和疏水性必须得到平衡,以实现高装载效率和制剂稳定性,同时确保API从制剂中有效释放。可供非消化道使用的辅料数量有限,这加剧了挑战。
例如,当使用表面活性剂或有机辅助溶剂来增加溶解度以实现高药物负荷时,可能会出现毒性问题和/或免疫原性反应。环糊精和其他辅料通过形成包合复合物来提高API的溶解度,这一过程受热力学的制约,也必须在高浓度下使用,这可能导致辅料的毒性问题。在某些情况下,通过纳米研磨进行颗粒大小的减少可能是减少提高溶解度所需的辅料浓度的有效方法。辅料浓度的降低可能会使药物含量更高,因为原料药仍处于固液分散状态,而不是被溶解在水溶液中。
一般来说,由于水溶性差通常是由原料药中存在的高度疏水区域造成的,因此在非消化道给药制剂中避免这些疏水区域与水环境接触被证明是提高溶解度的有效措施。许多增加溶解度的赋形剂因此具有相同的作用方式,即对疏水区的屏蔽作用,例如二氧化硅载体和聚合物胶束。
具有亲水和疏水分子的两亲赋形剂可以进行微调,对提高非消化道给药制剂中API的溶解度效果最好。除了聚合胶束外,纳米粒子制剂和脂质体制剂已被证明有助于疏水性小分子原料药的增溶。聚合物胶束和纳米颗粒通常可以实现更高的API负载。
一般来说,要使用各种辅料进行广泛的实验筛选,以找到合适的匹配。从药物的结构特性出发,有可能利用硅学模型来确定提高溶解度的策略。这种模型使科学家能够从有限的辅料小组开始,用实验设计的方法来提高溶解度。例如,如果原料药是疏水性的,赋形剂是乳化剂,那么原料药就会封存在乳化剂的疏水性核心中。事实上,具有疏水性基团和足够亲水性的赋形剂在水环境中共存,是有效的乳化剂和有用的增溶剂。聚山梨酯20和聚山梨酯80是非消化道治疗剂配方中常用的辅料。聚乙氧基化表面活性剂和聚乙二醇也被评估为在这些应用中提高溶解度的能力。
配制非消化道给药的难溶性原料药的一个首要考虑因素是,没有一个放之四海而皆准的赋形剂。目前仍在进行研究,目的是了解哪些原料药的特性有助于与不同辅料产生最佳的相互作用。辅料必须为每种原料药精心选择和微调。
在聚合物胶束中封装原料药
聚合物胶束的作用是将水溶性差的原料药封装在其内芯中,从而将药物物质从水环境中屏蔽掉。它们之所以有吸引力,有几个原因,包括聚合赋形剂往往有较少的毒性问题,与小链表面活性剂相比,在较高浓度下相对安全。许多还具有生物相容性,由氨基酸或其他存在于人体中的构件形成。
聚合物胶束可以由各种不同的聚合物类型组装而成,最受欢迎的选择包括聚乙二醇、聚氧化乙烯、硬脂酸和G-壳聚糖。所有这些聚合物都有疏水性区域,朝向胶束的核心,亲水性区域朝向外部水介质。这些聚合物表现出由疏水相互作用、静电相互作用和复合作用等力量引发的自组装行为。所产生的胶束的直径通常小于100纳米。

两亲生物可吸收的二嵌段共聚物,如聚(乙二醇)-甲基醚-嵌段聚(DL-乳酸)(mPEG-b-聚(DL-乳酸))和聚(乙二醇)-甲基醚-嵌段聚(DL-乳酸-co-甘醇)是常用的。当用这些聚合物配制时,疏水性的API与疏水性的乳酸/乙二醇聚合物段结合,而亲水性的PEG聚合物段则自行排列在周围的水环境中。
根据嵌段共聚物的分子量,形成了胶束或纳米颗粒。最后产生了极小的、高表面积的纳米胶束或纳米颗粒,这些胶束由外部亲水聚合物PEG段稳定。聚合物胶束和纳米颗粒的尺寸和物理特性改善了API的溶解度,并提高了API在患者中的暴露度。
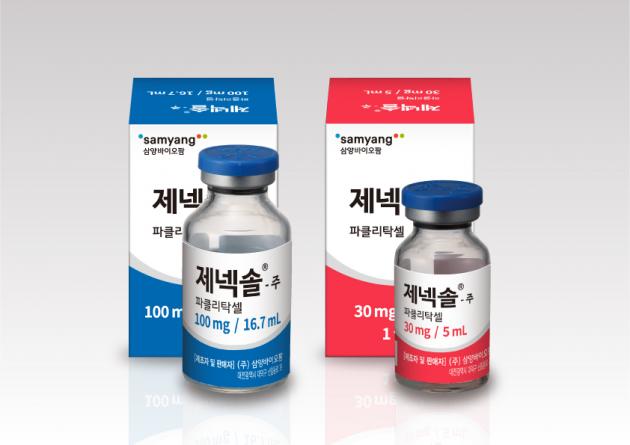
Genexol PM(Samyang Holdings)是最近推出的商业紫杉醇产品的一个例子,该产品使用20-50纳米的mPEG-b-聚(DL-内酰胺)聚合胶束配制。与含有表面活性剂的更多传统配方相比,它提供了48小时的持续释放,提高了溶解度和疗效,减少了毒性和过敏性。
聚合胶束和聚合纳米颗粒是有吸引力的制剂,其结合了高装载效率、有利的药代动力学特性和更好的临床疗效。生物相容性、生物可吸收的mPEG-b-聚乳酸二嵌段共聚物制成的聚合物胶束和聚合物纳米颗粒具有不小的未来潜力。
聚合物胶束是非消化道给药制剂的一个令人兴奋的技术进步。除了PEG化的聚乳酸、PEG化的聚乙醇酸,甚至乳酸和乙醇酸的组合等嵌段共聚物外,Polaxamers或Pluronics也被用于胶束的形成和溶解性的提高。这些三嵌段共聚物具有形成核心的更疏水的链条中心部分,更极性的亲水末端延伸到水环境中。
路博润生命科学健康提供了一种新的赋形剂技术,用于提高基于聚合物胶束的非消化道给药制剂的可溶性。其Apisolex赋形剂是一种多嵌段共聚物,包括一个聚肌氨酸嵌段和一个D-/L-混合聚氨基酸嵌段,肌氨酸是一种氨基酸衍生物,天然存在于人体肌肉和组织中,使其成为现有非消化道给药制剂中使用的赋形剂的生物相容性替代品,特别是在需要高药物负荷的地方。在Apisolex聚合物形成的聚合胶束中,混合聚氨基酸块形成疏水核心,而聚肌氨酸块形成亲水冠层。
LNP相似但结构不同
LNP也封装API,但它们在结构上与聚合物胶束不同。固体LNPs将疏水性的API置于固体核心中,即使颗粒分散在水环境中也保持固体。与此同时,纳米结构的囊泡由固体颗粒内的液体和固体脂质成分/区块组成。
LNP最近因其用于保护mRNA不被降解和帮助其细胞吸收而广为人知,它们对许多其他药物物质也是有利的。虽然mRNA和siRNA等核酸的溶解性并不差,但它们可以提高更传统的小分子API的溶解性。LNP可以为溶解性差的小分子提供更好的生物利用度和控制释放,在肿瘤学领域已经有许多文献报道的案例。LNP的未来在于开发新的功能性脂质,并实现对特定器官、组织和细胞的定位。
其他辅料
鉴于大多数新的候选药物在某种程度上都存在溶解度差的问题,许多工作都集中在确定一系列更广泛的解决方案来提高溶解度。对于非消化道给药制剂来说,环糊精是近年来被重新发现并越来越频繁地使用的赋形剂类型的一个例子。
这一环状低聚糖来自天然淀粉,以空心圆锥体的形式排列,外部亲水,内部疏水,因此可以从水介质中屏蔽各种疏水、水溶性差的API。环糊精表现出非常好的安全性,使其适合于非消化道给药。此外,环糊精还可以保护原料药免于化学降解,减少蛋白质的聚集,并掩盖气味和味道。Schäfer强调的一个例子是使用磺基乙醚-β-CD来配制remdesivir,一种用于治疗COVID-19的非消化道给药制剂。
白蛋白纳米颗粒和合成多肽及其他辅料作为非消化道给药制剂的溶解度增强剂已经引起了不少关注。
制剂之外
使用辅料来优化溶解度会带来一些挑战,因为这种类型的配方工作通常发生在开发周期的后半段。通常研发人员会发现,仅靠配方优化并不足以提高API的溶解度。因此,建议在开发过程中更早地解决API的溶解度问题。
这就需要研究API的加工,以提高药物的溶解度。除了通过纳米研磨来减小颗粒尺寸外,盐的形成、共晶体的形成和多晶体筛选也是重要的途径。这些方法不仅提供了显著提高溶解度的可能性,而且还可以解决物理和化学稳定性、溶解率和可加工性等特点。如果需要的话,还可以通过配方进一步优化。原料药加工和定制配方应该齐头并进,以实现候选药物的最佳成功概率。
新型辅料变得有吸引力
传统用于提高溶解度的新型辅料发展有限,研发人员倾向于使用已知安全状况的辅料创造新的配方技术,而不是开发新的辅料来提高溶解度。例如,使用已知毒性的现有聚合物开发新技术,如无定型固体分散技术,比开发新的辅料来提高难溶性药物的溶解度要多很多。
然而,最近新型辅料也正在成为一种有吸引力的途径,提供了一种利用现有技术并实现相同甚至更好结果的方法。新型辅料还提供了更多的知识产权保护,而且由于知识产权是新的,药物开发商和营销商可以利用更长的专利期。新的赋形剂知识产权对以前因溶解度问题而被搁置的老的临床候选药物可能特别有用。
高分子赋形剂,特别是那些能够实现胶束配方的赋形剂,就是一个很好的例子。这些新辅料为以前在药物开发过程中失败的原料药实现更好的溶解度和高药物负荷提供了重要手段。使用美国FDA的505(b)(2)监管途径也允许用新型辅料重新配制以前批准的药物,以提高生物性能,但降低应用风险,加快上市时间。
作者:Cynthia A. Challener
来源:Excipients for Solubility Enhancement of Parenteral Formulations, Pharmaceutical Technology 46 (11) 2022.
来源:荣格-《国际医药商情》
原创声明:
本站所有原创内容未经允许,禁止任何网站、微信公众号等平台等机构转载、摘抄,否则荣格工业传媒保留追责权利。任何此前未经允许,已经转载本站原创文章的平台,请立即删除相关文章。